Procés isocor

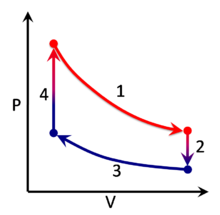
Un procés isocor, també anomenat procés isocòric, és un procés termodinàmic en el qual el volum es manté constant;[1] . Això implica que el procés no produeix treball:
- ,
on P és la pressió (el treball és positiu, ja que és exercit pel sistema).
Càlculs del procés
Càlcul del treball (W)
Ja que no hi ha desplaçament el treball realitzat pel gas és nul.
Càlcul de la variació d'energia interna (ΔU)
Aplicant la primera llei de la termodinàmica, podem dir que ΔU (la variació de l'energia interna del sistema) és:
en un procés isocor, és a dir a volum constant, tota la calor que transferim al sistema augmentarà la seva energia interna U.
Càlcul del calor absorbit
Si la quantitat de gas es manté constant, llavors l'increment d'energia serà proporcional a l'increment de la temperatura,
on CV és el calor específic molar a volum constant.
Vegeu també
Referències
- ↑ «Procés isocor». Gran Enciclopèdia Catalana. Barcelona: Grup Enciclopèdia Catalana.
Enllaços externs
- Termodinámica. Proceso isócoro Arxivat 2012-04-13 a Wayback Machine.(castellà)







